Monthly Archives: October 2016
Coryza du chat
Le coryza du chat est une maladie complexe, car elle n’est pas due à un seul microbe, mais à l’association de plusieurs virus et de bactéries.
Trois virus sont impliqués dans le coryza et provoquent chacun des symptômes différents :
- Un virus de la famille des « Herpes virus » responsable d’une infection du nez et des voies respiratoires. Les symptômes sont : toux, éternuements, importants écoulements au niveau des yeux et du nez, conjonctivite et faiblesse de l’état général (perte d’appétit et fièvre). C’est le virus le plus dangereux. Il peut être mortel chez des animaux affaiblis si l’on ne met pas en place un traitement rapide.
- Un Calicivirus provoquant lui aussi de la fièvre et de l’abattement, des écoulements oculo-nasaux et surtout des ulcères dans la bouche (plaques rouges très nettes sur la langue ou les gencives). Ces plaies dans la bouche sont douloureuses et provoquent salivation importante et perte d’appétit.
- Un Réovirus bénin qui provoque quelques larmoiements.
A ces atteintes virales il faut ajouter les bactéries qui très souvent se surajoutent et provoquent des complications chez les chats déjà affaiblis. Le chat présente alors du pus dans les yeux et le nez.
Les principaux symptômes
Cette maladie touche en priorité les animaux vivant en communauté (chatterie, refuge, « famille nombreuse », chats semi-sauvages), les chatons et les adultes non vaccinés.
Après une incubation courte (2 à 5 jours), les signes respiratoires (toux, éternuements), les écoulements des yeux et du nez, la perte d’appétit et parfois les tâches rouges dans la bouche apparaissent, de manière plus ou moins importante selon les animaux.
Si plusieurs chats présentent les mêmes symptômes au même moment, il est fort probable qu’il s’agit du coryza qui est une maladie très contagieuse. La contagion s’effectue, (comme pour la grippe chez l’homme), sans contact direct, par les éternuements ou quand les chats se soufflent dessus.
La maladie non traitée peut évoluer vers une guérison naturelle chez certains animaux résistants. Mais attention elle peut quelquefois se compliquer d’une nécrose des os du nez, avec infection généralisée, et finir par la mort de l’animal si celui-ci est déjà affaibli et refuse de s’alimenter.
Un chat guéri du coryza peut rester porteur de longues années, et être à nouveau contagieux à la suite d’évènements tels qu’un stress, une mise-bas ou une autre maladie.
Migraine
«Hypersensible à tout»
Le migraineux en crise ne supporte plus rien, ni la lumière, ni le bruit, ni les odeurs, ni la moindre alimentation ; il est nauséeux et parfois vomit. Il se décrit souvent lui-même comme «une véritable loque». La crise dure de quelques heures à trois jours, se terminant souvent par un sommeil réparateur.
Entre les crises, le migraineux ne souffre pas mais il est «hypersensible à tout»: ce qu’il mange ou boit, le temps qu’il fait, les émotions qu’il ressent, les variations hormonales (chez la femme), les changements de rythme de vie, la grasse matinée, l’altitude, etc.
Cette hypersensibilité est liée à une hyperexcitabilité des neurones du cortex cérébral que le migraineux gardera toute sa vie, même si elle va se réduire en vieillissant, expliquant les diminutions habituelles de la fréquence et de la sévérité des crises avec l’âge.
Parfois le mal de tête est précédé pendant vingt à trente minutes de phénomènes visuels à type soit de formes élémentaires brillantes telles que zigzags, éclairs, lignes brisées, étoiles, soit de flou dans tout ou partie du champ visuel, avec souvent une zone centrale quasiment aveugle au contour brillant crénelé, appelée scotome scintillant. Ces phénomènes s’accroissent en intensité et en étendue au fil des minutes en une progression caractéristique qualifiée de «marche migraineuse». Il peut s’y associer des picotements ou des fourmillements également progressifs d’un côté du corps et parfois des difficultés de langage (aphasie). Ces phénomènes sont qualifiés d’aura neurologique: il existe ainsi des crises avec ou sans «aura», un migraineux pouvant n’avoir soit qu’un seul type de crise (le plus souvent sans aura), soit les deux.
Typiques ou Atypiques
Lorsque les crises sont atypiques, que les maux de tête persistent entre les crises, qu’il y a d’autres symptômes neurologiques, que les crises ne ressemblent pas aux crises habituelles, rien ne sert de parler de «fausse migraine», un avis spécialisé et des examens complémentaires sont nécessaires à la recherche d’une autre cause éventuelle de mal de tête.
Que la migraine soit typique ou atypique, qu’il s’agisse d’un enfant ou d’un adulte, la première consultation d’un migraineux est nécessairement longue puisque la description détaillée des crises, l’examen clinique, le recueil des facteurs déclenchants, les explications sur la nature de la migraine et ses diverses modalités thérapeutiques, l’organisation du suivi ne requièrent pas moins de trente minutes à une heure !
Hyper-nauséeux familial
L’hyper nauséeux familial est une réaction exacerbée à certaines odeurs ou certains aliments due à une hypersensibilité des organes du goût et de l’odorat. Cette hypersensibilité à caractère variable selon les individus est probablement génétiquement déterminée.
Chez l’enfant, les troubles associés sont les régurgitations et vomissements récurrents, les troubles alimentaires de type inappétence lenteurs et aversions avec pour corollaire un développement pondéral médiocre, et enfin des troubles de l’articulation de la parole.
Développement du goût et de l’odorat chez le foetus et le jeune enfant
Papilles gustatives et système olfactif sont matures chez le fœtus dès les premières déglutitions de liquide amniotique (LA) et ce, dès la 11° semaine de vie intra utérine.
Le système olfactif est composé de 2 organes : l’épithélium olfactif et l’organe voméro-nasal.
Le premier perçoit les substances odorantes volatiles environnementales et nutritives et le second serait, semble-t-il plus spécialisé dans la perception des phéromones.
La langue, elle, est l’organe du goût, elle perçoit les quatre saveurs: sucré, salé, acide, amer. Elle a surtout une perception très fine des températures, des formes et consistances, ce que nous appelons en neurologie les stéréognosies linguales. La langue ne perçoit pas les odeurs, c’est ainsi que ce que nous appelons le “goût” est constitué à 80% d’odorat.
Chez le fœtus et le jeune enfant ces deux organes des sens sont très développés. Le fœtus pendant près de 6 mois va percevoir les phéromones maternelles et le goût et l’odeur du LA. Ce liquide est à température constante, il est visqueux et il va varier de goût en fonction de ce que la mère a ingéré. A la naissance, une fois le cordon ombilical coupé, l’enfant posé sur sa mère sera immédiatement plongé dans un milieu familier et rassuré. Il existe en effet un autre cordon reliant l’enfant à la mère qui, s’il est invisible n’en est pas moins bien réel. Ce cordon est le cordon sensoriel olfactif et gustatif.
Grâce à son organe voméro-nasal, l’enfant va reconnaître les phéromones maternelles qu’il connaît déjà, et il va se diriger vers le mamelon guidé par son organe olfactif pour prendre sa première tétée. Le colostrum puis le lait sont très proches de ce qu’il a perçu et mémorisé pendant sa vie intra utérine en déglutissant du LA (Schaal). Il SAIT déjà, de par son expérience sensorielle intra-utérine, reconnaître le bon aliment du “poison”. Tout aliment autre que le lait à bonne température (35/36°) va être immédiatement repéré par les organes du goût et de l’odorat et un processus de défense va s’enclencher afin de ne pas avaler ce produit étranger qui pourrait être du “poison”.
Pour la majorité de la population, le rôle du nauséeux est donc d’inverser brutalement le processus de déglutition dès que les papilles gustatives ou le système olfactif détecte une substance nocive et ce, afin de ne pas l’avaler. Il y a cependant des différences de comportement face à des aliments nouveaux, ce qui amène à une autre notion qui est la celle de variation individuelle des sensibilités olfactives et gustatives.
La répartition des différentes sensibilités olfactives et gustatives chez les individus se fait sur le modèle d’une courbe de Gauss. Les personnes les plus sensibles, au seuil de détection très bas, perçoivent d’infimes quantités de substances odorantes volatiles (par exemple les “nez” dans l’industrie cosmétique, aux capacités perceptives exceptionnelles). A l’inverse, certaines personnes ne perçoivent les substances odorantes qu’à un taux de concentration très élevé ce qui est le signe d’un seuil de détection très élevé.
Les “super goûteurs” et “super nez” qui représentent 25% de la population, les “goûteurs et nez moyens” : 50% de la population, les “goûteurs et nez faibles”: 25% de la population (on dit que ce groupe présente une anosmie partielle ou élective).
Troubles de l’Odorat
L’odorat et le goût font partie des sens qui, grâce à leur analyse chimiosensorielle, nous permettent de discriminer des substances chimiques.
L’odorat et le goût sont des sens vitaux. Ils contribuent non seulement à la qualité de vie mais permettent également aux individus, pour ne citer que quelques exemples, de détecter suffisamment tôt un incendie ou de les empêcher de manger un aliment avarié. Par ailleurs, la perte de l’odorat entraîne également des difficultés sociales non négligeables, si ce n’est que pas l’impossibité de sentir sa propre odeur corporelle.
L’odorat et le goût réposent sur des molécules qui sont libérées par des objects faisant partie de l’environnement. Par la suite, ces molécules stimulent certaines cellules nerveuses implantées dans la bouche ou le nez. Ces cellules nerveuses à leur tour transmettent les signaux au cerveau où les odeurs et le goût sont perçus et identifiés.
Les troubles du goût sont rares. Seuls 5% des patients souffrent effectivement de troubles du goût; la grande majorité est atteinte de troubles de l’odorat.
Les troubles de l’odorat sont de diverses origines. Le sens de l’odorat peut être :
- accru (hyperosmie),
- diminué (hyposmie),
- perdu (anosmie)
Il est possible de :
- Une odeur agréable est perçue comme désagréable (cacosmie),
- Une odeur désagréable est perçue comme agréable (euosmie),
- Altération de la perception des odeurs en présence d’une stimulation. La plupart du temps, les parfums sont perçus comme des odeurs désagréables (par exemple une rose est sentie comme une autre chose) (parosmie)
- avoir des hallucinations olfactives ( hallunosmie)
- Perception d’odeurs en l’absence de stimulation (on sent quelque chose qui n’est pas là) -Le plus souvent, ce sont des odeurs désagréables qui sont perçues (phantosmie)
Troubles du goût
-
Agueusie: Perte complète du sens du goût
-
Hypogueusie: Sens du goût diminué
-
Hypergueusie: Exacerbation du sens du goût ou hypersensibilité aux goûts
- Paragueusie: Altération de la perception du goût en présence d’une stimulation (par exemple quelque chose de sucré a soudain un goût amer).
- Phantogueusie: Perception de goût en l’absence de stimulation (on a le goût de quelque chose qui n’est pas là).
Le syndrome de la bouche brûlante (burning mouth syndrom) représente un tableau clinique à part entière pouvant également entraîner des troubles du goût, caractérisé par une sensation de brûlure dans la bouche ou sur la langue, accompagnée de fourmillements ou de prurit.
Quel mécanisme ?
Le goût et l’odorat sont intimement liés dans leur fonctionnement et leurs anomalies retentissent l’un sur l’autre.
La distinction des odeurs dépend de l’arôme stimulant les récepteurs de l’odorat (chémorécepteurs olfactifs).
La perte ou la réduction de l’odorat est l’atteinte la plus commune et s’accompagne fréquemment d’un trouble du goût. Il y a deux façons d’altérer l’odorat :
- En empêchant l’odeur d’arriver à la zone sensible du nez, par atteinte transmissionnelle quand les molécules odorantes ne peuvent plus entrer en contact avec les cellules olfactives ;
- En empêchant l’information nerveuse d’arriver au cerveau afin qu’elle y soit interprétée par atteinte de perception d’une lésion nerveuse qui peut siéger en divers endroits, des cellules olfactives au centre nerveux olfactif (dans le cerveau) en passant par le nerf olfactif lui-même.
Quelles causes ?
Les troubles de l’odorat peuvent être de deux origines : atteinte transmissionnelle et atteinte de perception.
- Par atteinte de la transmission
Les troubles de l’odorat par ce type d’atteinte sont souvent l’objet d’une anomalie anatomique qui empêche les odeurs de parvenir à la partie sensible du nez. La mauvaise qualité de mucus (qui recouvre les cellules sensorielles) ou bien d’un obstacle placé dans le nez (corps étranger, polypes, tumeurs…) représentent presque la moitié des causes des troubles de l’odorat.- La polypose naso-sinusienne est certainement la cause la plus typique. Les polyposes nasales, bénignes, atteignent souvent les deux narines avec une atteinte de la muqueuse qui présente des œdèmes bouchant le nez et altérant l’odorat.
- Même exceptionnelle une mucoviscidose doit être recherchée.
- La rhinite peut être aiguë avec un syndrome grippal et donc transitoire . Elle peut aussi être chronique, allergique avec rhinorrhée, éternuements, congestion nasale et prurit voire conjonctivite ou non allergique
- Les pathologies naso-sinusiennes de type inflammatoire provoquent les rhino-sinusites qui associent, à des degrés variables, l’écoulement du nez à une obstruction nasale bilatérale, des éternuements et des troubles de l’odorat.
- Les sinusites s’accompagnent d’anosmie dans les formes chroniques touchant tous les sinus. Le diagnostic sera fait à l’aide d’un scanner
- Par atteinte de perception
Les traumatismes, provoqués par un accident ou à la suite d’une intervention chirurgicale, se traduisent par une perte généralement complète de l’odorat, avec un trouble du goût souvent associé.- Les intoxications médicamenteuses ( médicaments anti-cancéreux , morphine , sels d’or , L dopa ..) et certains polluants industriels
- Les causes tumorales avec des localisation à la base du crane
- Les maladies neurologiques avec en particulier la maladie D’Alzheimer où les troubles de l’odorat pourraient être un facteur précoce de diagnostic mais aussi la maladie de parkinson et l’épilepsie
Autres causes des troubles de l’odorat :
- Troubles hormonaux
- Affections dentaires
- Produits chimiques, médicaments
- Radiothérapie en cas de tumeurs de la tête et du cou
- Maladies neurologiques comme la sclérose en plaque, le Parkinson ou la maladie d‘Alzheimer.
- Maladies métaboliques comme le diabète sucré.
- Maladies thyroïdiennes, carence en vitamine B12, en vitamine A ou en zinc.
- Cancer de la région ORL
- Maladies psychiques: dépression, schizophrénie
- Causes congénitales
Les causes les plus fréquentes de troubles du goût sont :
- Traumatisme crânio-cérébraux
- Infections des voies respiratoires supérieures
- Exposition à des substances toxiques
- Traitement dentaire
- Radiothérapie
- Médicaments
Autres causes de troubles du goût :
- Tumeurs, boulimie, maladies thyroïdiennes, diabète sucré, maladies rénales et hépatiques.
- Une mauvaise hygiène buccale peut également favoriser des troubles du goût.
- Troubles (symptômes)
Les termes ”troubles de l’odorat” (dysosmies) et ”troubles du goût” (dysgueusies) décrivent différents troubles de la perception des odeurs et des goûts. On distingue les troubles quantitatifs et des troubles qualitatifs.
Fibrose pulmonaire
La fibrose pulmonaire est une lésion des poumons caractérisée par une fibrose, c’est-à-dire la présence d’un excès de tissu conjonctif fibreux. De nombreuses pathologies sont en cause, parmi les pneumopathies interstitielles. La gêne respiratoire (dyspnée) est le principal symptôme. Le plus souvent la présentation clinique et l’aspect du scanner permettent de poser le diagnostic. Le traitement est celui de la cause et consiste à prévenir l’aggravation de la maladie.
Causes
La fibrose pulmonaire est un stade évolutif de plusieurs maladies, la plupart d’entre elles étant classées dans les pneumopathies interstitielles.
Les maladies et les conditions qui peuvent causer la fibrose pulmonaire comprennent :
- l’inhalation de polluants environnementaux ou sur le lieu de travail1, comme dans le cas de l’asbestose ou de la silicose, ainsi que l’exposition à certains gaz, les mineurs, les marins et les sableurs, entre autres, sont des catégories à risque plus élevé ;
- une pneumopathie d’hypersensibilité résulte le plus souvent de l’inhalation de poussières contaminées par des sources bactériennes, fongiques ou animales ;
- le tabagisme peut accroître le risque ou aggraver les symptômes ;
certaines maladies auto-immunes comme la polyarthrite rhumatoïde, le lupus érythémateux disséminé et la sclérodermie ; - d’autres maladies du tissu conjonctif comme la sarcoïdose et la granulomatose de Wegener ;
des infections ; - certains médicaments comme l’amiodarone, la bléomycine, le busulfan, le méthotrexate et le nitrofurantoïne ;
- la radiothérapie mammaire.
Dans certains cas, la fibrose pulmonaire peut apparaître sans cause connue. Il s’agit de pneumopathie interstitelle diffuse idiopathique, dont la principale forme est la fibrose pulmonaire idiopathique.
Pour une partie des patients, il y a un nombre croissant d’indications qui tendent à individualiser la fibrose pulmonaire familiale, avec prédisposition génétique. Par exemple, une mutation dans la protéine surfactante C a été constatée dans certaines familles atteintes.
Papillomavirus humain
Le virus du papillome humain (VPH, en anglais Human papillomavirus, HPV) est un virus à ADN faisant partie de la famille des Papillomaviridae. Il est responsable des infections sexuellement transmissibles les plus fréquentes puisque l’estimation des personnes actuellement contaminées par ce virus est comprise entre 10 et 30 %.
Il existe environ 200 génotypes de papillomavirus. Certains génotypes se transmettent par voie sexuelle et infectent les muqueuses génitales, d’autres se transmettent par contacts cutanés et infectent la peau.
Les manifestations cliniques les plus connues de la contamination sexuelle sont les condylomes acuminés (dits également « verrues génitales », ou « végétations vénériennes » ou « crêtes de coq »), déjà décrits par Hippocrate. Mais la gravité de cette infection est que certains génotypes sont le facteur obligatoire du cancer du col de l’utérus, découverte qui valut à Harald zur Hausen le Prix Nobel de physiologie ou médecine 2008.
Les manifestations cliniques cutanées de l’infection à VPH comprennent les verrues vulgaires et les verrues plantaires.
Virus
Virus nu, il est particulièrement résistant dans le milieu extérieur (froid, solvants organiques, détergents). Son génome est constitué de 8 000 paires de bases. Le virion est non enveloppé, la capside est à symétrie cubique constituée de 72 capsomères en structure icosaédrique, de 55 nm de diamètre ; il possède un ADN bicaténaire, circulaire, fermé, à réplication dans le noyau cellulaire.
Ce virus a un tropisme pour les épithélium malpighiens.
Les papillomavirus humains appartiennent surtout au genre α-Papillomavirus. On en compte plus de 200 génotypes. 120 ont été identifiés et séquencés1. Ils ont une spécificité d’hôte étroite (spécifique d’une espèce), ainsi qu’une spécificité de tissus.
Ils sont désignés par un nombre en fonction de leur chronologie historique de découverte.
Il existe trois grands groupes :
- types muqueux et génitaux à potentiel cancérigène élevé : HPV-16, 18, 31, 33, 35, 45, 51, 52, 58, etc.
- types muqueux et génitaux à faible potentiel cancérigène : HPV-6, 11 (papillomes et condylomes acuminés ano-génitaux)
- types cutanés : HPV-1, 2, 3, 4, 5, 7, 8, 10, 27, 57, 60, etc.
Le génome des virus génitaux codent huit gènes (et autant de protéines).
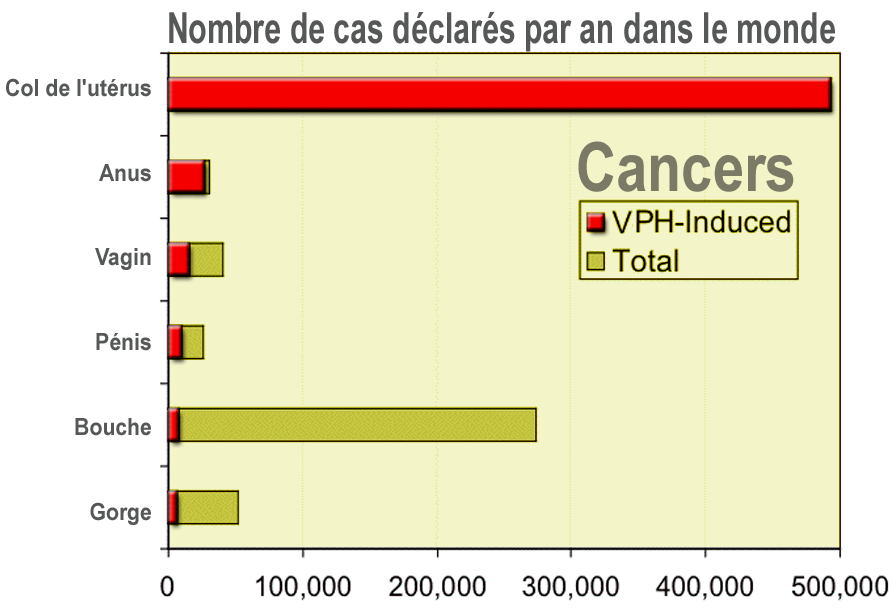 Epidémiologie
Epidémiologie
Les papillomavirus humains sont souvent présents sur la peau normale de sujets sains. On parle d’infections cutanées asymptomatiques, qui apparaissent très tôt dans l’enfance. La plupart des infections à papillomavirus sont latentes ou transitoires. Les lésions induites par ces virus régressent spontanément la plupart du temps.
Infections génitales
Ce sont les infections génitales qui ont été les plus étudiées. Le VPH est la principale cause d’infections sexuellement transmissibles (IST) aux États-Unis4. Bien que sa prévalence5 soit élevée (près de 25 % de la population féminine pubère, elle est particulièrement importante chez la jeune femme de moins de 20 ans) :
- plus de la moitié des lésions de bas degré régressent spontanément en quelques années, 10% évoluant vers des lésions de haut degré ;
- environ un tiers des lésions de haut degré régressent spontanément, 5 % évoluant vers un cancer ;
- au total, 5 % des infections évoluent vers un cancer.
On considère ainsi que la majorité des personnes sexuellement actives ont eu au moins une infection à papillomavirus à potentiel cancérogène élevé au cours de leur vie, surtout au cours des premières années de la vie sexuelle.
Le virus se transmet par contact direct avec une peau ou une muqueuse contaminée, par voie buccale, auto-inoculation (la transmission de verrues vulgaires est favorisée par le grattage) et par contact indirect (objets, surfaces contaminés, locaux – douches, hammams, sièges de toilettes, piscines, etc. – favorisent la propagation des verrues plantaires) ; la transmission est sexuelle dans le cas des condylomes ano-génitaux ; la transmission du papillome laryngien s’effectue de la mère à l’enfant lors du passage dans la filière génitale.
De 1 % à 2 % des hommes et des femmes infectés présenteront des condylomes exophytiques cliniquement visibles.
Les lésions exophytiques cliniquement visibles sont rarement associées au cancer : seuls certains génotypes du VPH sont associés aux cancers du col de l’utérus, de la vulve, du pénis et au cancer anorectal. L’ADN de certains sérotypes d’HPV serait présent dans au moins 80-90 % des lésions cervicales dysplasiques (néoplasies cervicales intra-épithéliales) et des cancers du col de l’utérus (HPV 16, 18, 31, 33 ou 35). Les génotypes (HPV 6 et 11) qui causent le plus souvent les condylomes exophytiques n’ont pas été associés à ces cancers.
La transmission périnatale d’une infection symptomatique semble rare. Lorsqu’elle survient, l’infection est associée à des lésions génitales et à des lésions des cordes vocales. On ignore la durée de la période d’incubation. Habituellement, la transmission périnatale devient cliniquement apparente au cours des deux premières années de vie.
Autres infections
Le papillomavirus humain (HPV) est également retrouvé au niveau d’autres épithéliums malpighiens9, de la muqueuse oropharyngée mais surtout de la muqueuse œsophagienne. HPV y est souvent observé au sein de lésions bénignes ou malignes où il induit la formation des cellules pathognomoniques de l’infection : les koïlocytes.
Tumeurs bénignes de l’œsophage
Les lésions bénignes au niveau de l’œsophage sont des papillomes viraux (squamous cell papillomas, SCP).
L’implication de HPV est fortement suspectée au vu de l’existence d’une koïlocytose plus ou moins prononcée dans ces lésions, mais la preuve n’en est apportée par PCR que dans 20 % des cas (0 % dans les pays à faible risque par exemple la Finlande, supérieur à 50 % dans les pays à haut risque par exemple la Chine lors d’une campagne de dépistage du cancer de l’œsophage.
Ceci permet de penser que HPV (essentiellement les types 6, 11 et 16), s’il n’est pas suffisant pour induire la formation de papillomes, a très certainement un rôle de cofacteur dans l’apparition de ces tumeurs bénignes (Chang et al. 1991).
Il semble que très peu de papillomes puissent évoluer vers un carcinome épidermoïde.
Tumeurs malignes de l’œsophage
Les tumeurs malignes de l’œsophage sont des carcinomes de type épidermoïde ; les adénocarcinomes se développent quant à eux au niveau d’un œsophage de Barrett. HPV semble fortement impliqué dans l’étiologie des carcinomes épidermoïdes de l’œsophage (squamous cell carcinoma, SCC) : on y retrouve également des koïlocytes.
La première étude prouvant le rôle d’un papillomavirus dans la genèse de lésions œsophagiennes est une étude animale. Les bovins des Highlands en Écosse présentent fréquemment des papillomes œsophagiens; expérimentalement, une papillomatose a été induite par le papillomavirus bovin 4 (BPV4). Ces animaux développent fréquemment des cancers de l’œsophage, et 96 % des animaux qui présentent ce cancer sont également porteurs de papillomes BPV4-induits. On a démontré que l’ingestion de fougères (qui sont riches en carcinogène et en immunosuppresseurs, par exemple l’azathioprine) était un facteur de la transformation maligne des papillomes16.
Chez l’homme, on retrouve fréquemment HPV par PCR dans les SCC (de 25 % à 40 % dans les études) de type 6, 11, 16, 18 et 30, mais le plus souvent de type 1617. Comme pour les lésions bénignes, on retrouve plus fréquemment HPV dans les coupes de SCC en provenance de pays à risque élevé ou à haut risque, que dans celles provenant de pays à faible risque.
Il est actuellement admis que HPV n’est qu’un cofacteur de carcinogénèse en ce qui concerne les carcinomes épidermoïdes de l’œsophage, agissant en synergie avec d’autres facteurs de risque (nitrosamines, mycotoxines, consommation d’opium, de tabac, d’alcool, etc.).
Manifestations cliniques de l’atteinte génitale
L’infection peut être subclinique ou clinique, mais elle est habituellement asymptomatique.
Chez la femme, le col de l’utérus est l’endroit du corps le plus fréquent d’infection génitale au VPH. L’infection en atteint souvent plusieurs (le col de l’utérus, le vagin, la vulve, etc.). Le papillomavirus peut également créer des problèmes génitaux chez l’homme (verrues anogénitale sur le court terme, cancer du pénis sur le long terme) 20,21.
Condylome plan
Les lésions kératinisées légèrement surélevées.
- Condylome acuminé : Des excroissances sur la peau ou les muqueuses de la région ano-génitale sont souvent multiples et polymorphes avec apparence exophytique variant entre une excroissance digitiforme ou en chou-fleur et une lésion papuleuse.
L’histoire naturelle de l’infection est marquée par une fluctuation de la taille et du nombre des condylomes et, dans bien des cas, par leur éventuelle disparition. La taille et le nombre des condylomes peuvent croître durant la grossesse.
Pouvoir pathogène et génotype
Le pouvoir pathogène des papillomavirus humains dépend :
- du statut immunitaire de la personne infectée : les déficits immunitaires favorisent ce type d’infection (immunodépression congénitale, transplantations, VIH, traitements immuno-suppresseurs) ;
- de facteurs génétiques favorisant la transformation maligne des lésions dues aux HPV ;
- du type d’HPV :
- les types HPV 6 et HPV 11 causent des lésions cutanées et muqueuses bénignes (verrues vulgaires, verrues plantaires, verrues planes, condylomes ano-génitaux, verrues génitales, épidermodysplasie verruciforme et papillomes laryngiens);
- les types HPV 16, 18, 31, 33 et 35 sont associés à des néoplasies cervicales intra-épithéliales et au cancer du col de l’utérus.
| Lésions | Type de papillomavirus |
|---|---|
| Lésions cutanées | |
| Myrmécie | 1 |
| Verrues vulgaires | 2-4-29-75-76-77 |
| Verrues planes | 3-10-28 |
| Verrues intermédiaires | 10-26-27-28-29 |
| Verrues des bouchers | 7 |
| Maladie de Bowen | 34 |
| Kératoses actiniques | 36 |
| Kératoacanthome (un seul cas) | 37 |
| Mélanome (un cas) | 38 |
| Carcinome spinocellulaire | 41-48 |
| Lésions précancéreuses | 49 |
| Papillome maxillaire inversé | 57 |
| Kyste épidermoïde plantaire | 60 |
| Verrue myrmécie kystique | 63 |
| Verrues pigmentées | 65 |
| Lésions bénignes de l’épidermodysplasie verruciforme | 5-8-9-12-14-15-17-19-20-22-23-24-25-36-46-47-49-59 |
| Cancers de l’épidermodysplasie verruciforme | 5-8-20-47 |
| Lésions des muqueuses | |
| Condylomes de la muqueuse génitale | 6-11-54 (BR) |
| Néoplasie intraépithéliale anogénitale | 34-40-42-43-57-59-61-62-64-67-68-69 (BR) |
| Papulose bowénoïde | 34-55 (BR) |
| Papillome vulvaire | 42-70 (BR) |
| Hyperplasie vulvaire | 43 (BR) |
| Condylomes anogénitaux | 44 (BR) |
| Néoplasie intraépithéliale anale | 71-74 (BR) |
| muqueuse orale : maladie de Heck | 12-32 (BR) |
| papillomes oraux (immunodéprimés) | 72-73 (BR) |
| Cancer anogénital | 16-18-30-31-33-35-39-45-52-56-58-66 (HR) |
| Néoplasie intraépithéliale anogénitale | 35-39-45-52-56-58-69 (HR) |
| Néoplasie intraépithéliale et cancers génitaux | 51 (HR) |
| Cancers oraux et laryngés | 30 (HR) |
Verrue
La verrue est une petite excroissance de la peau ou une petite lésion qui peut être induite par un microtraumatisme, et peut apparaître sur presque toutes les régions du corps. On peut la retrouver sur la main, le coude, le genou, le visage, le pied ainsi que sur les organes génitaux.
Les verrues sont des tumeurs cutanées bénignes (non cancéreuses). Elles ont pour origine l’infection de la peau par un virus, le papillomavirus humain (HPV) dont on dénombre une cinquantaine de types différents.
On distingue plusieurs types de verrues :
- les verrues vulgaires le plus souvent dues aux HPV 2 et 4,
- les verrues planes dues aux HPV 3, 10 et 28,
- les verrues plantaires, qui peuvent être uniques, profondes et douloureuses à la marche (myrmécie due à HPV 1), ou multiples et contiguës (mosaïque due à HPV 2),
- les papillomes verruqueux,
- les verrues génitales, les condylomes,
- les kystes épidermoïdes à inclusions ou papillomes kystiques exclusivement dus à HPV 60.
Microscopie
Le caractère principal retrouvé en histologie est une vacuolisation des kératinocytes de la couche granuleuse et des couches supérieures de l’épiderme. On note des inclusions basophiles composées par les particules virales et des inclusions éosinophiles contenant une kératine anormale.
Dans la verrue vulgaire, il existe une hyperplasie épidermique à limites nettes qui associe une hyperacanthose et une hyperkératose ; l’altération fondamentale qui distingue la verrue des autres papillomes est la présence de remaniements cellulaires dans le corps muqueux de Malpighi : les cellules perdent leurs ponts d’union et apparaissent volumineuses, à cytoplasme vacuolaire, à noyau foncé pycnotique.
Verrues vulgaires
Les verrues vulgaires sont des formations tumorales épidermiques à bord net ; leur surface est rugueuse, kératosique. Leur taille varie de 1 à plusieurs millimètres. Des lésions très proches l’une de l’autre peuvent être confluentes.
Elles peuvent siéger sur l’ensemble du revêtement cutané, mais on les retrouve préférentiellement sur le dos des mains et sur la face d’extension des doigts. On note parfois un phénomène de Koebner (localisation des verrues sur des sites de traumatismes). Une verrue sous-unguéale ou périunguéale peut retentir sur la conformation de l’ongle et le déformer.
Les verrues des bouchers et des poissonniers sont un cas particulier : elles sont spécifiquement dues à HPV 7 alors que ce virus n’a jamais été isolé chez les animaux manipulés.
Verrues planes
Les verrues planes sont de petites formations prenant l’allure de papules de petite taille (3 à 4 mm de diamètre en général) de couleur contrastant peu avec la peau avoisinante (rose ou chamois). Leur surface peu kératosique est lisse. Elles se situent essentiellement au niveau du visage ou des membres supérieurs.
Verrues plantaires
Les verrues plantaires sont des verrues qui ont leur siège au niveau des points d’appui du pied. Les verrues disparaissent souvent toutes seules, mais le traitement abrège la période douloureuse et diminue le risque de contagion pour l’entourage.
Ce sont des tumeurs bénignes mais contagieuses, qui résultent d’une prolifération de cellules de l’épiderme. L’agent causal est un papillomavirus de type 1, 2, 4, 7 ou 63 (ces types sont classés sur la base des symptômes clinique visibles).
Elles sont plus rares chez les adultes car leur immunité acquiert une capacité de défense contre ces virus.
On suppose que le virus pénètre la peau via de minuscules coupures ou écorchures dans la couche cornée de la peau du pied. Les verrues ne deviennent visibles que plusieurs semaines ou plusieurs mois après l’infection. En raison de la pression sur la plante des pieds, la verrue est repoussée vers l’intérieur et peut être recouverte d’une couche de peau dure. Une verrue plantaire peut devenir très douloureuse si elle n’est pas traitée.
On décrit deux types de verrues plantaires :
- les myrmécies, qui sont des tumeurs profondes, douloureuses, localisées aux points d’appui (associées à HPV 1);
- les verrues plantaires en mosaïque, plus superficielles et même en relief, indolores, siégeant habituellement hors des points d’appui (associées à HPV 2).
Une confusion est parfois possible avec les durillons, oignons, ou les cors.
Les verrues plantaires sont souvent très douloureuses à la pression et à leur endroit, les stries de la peau (dermatoglyphes) sont interrompues. À maturité, elles sont constituées d’un centre blanchâtre qui s’enfonce profondément dans le derme, entouré d’une couronne kératinisée très importante.
Vue à la loupe, une verrue évoque souvent une forme de fleur, avec de minuscules pétéchies foncés ou des taches thrombosées évoquant des capillaires dans leur centre. Des saignements peuvent survenir si elles sont éraflées.
Papillomes verruqueux
Ce sont les verrues filiformes qu’on retrouve chez l’homme au niveau de la barbe; elles sont habituellement disséminées par le rasage. On peut en retrouver au niveau des paupières.
À signaler le cas particulier de la papillomatose cutanée floride : il s’agit de l’apparition rapide de nombreux papillomes verruqueux n’importe où sur l’ensemble du revêtement cutané, très souvent associée à un acanthosis nigricans. Cette entité entre dans le cadre des syndromes paranéoplasiques accompagnant ou pouvant révéler un cancer viscéral.
Papillomes kystiques
Les kystes épidermoïdes se présentent comme des verrues plantaires, mais avec conservation des dermatoglyphes.
Verrues génitales
Les condylomes (végétations vénériennes) sont sexuellement transmissibles (IST) et issues du papillomavirus humain.
Deux types de lésions dermatologiques peuvent prendre un aspect proche de celui des verrues :
- les Molluscum contagiosum sont des papules hémisphériques et translucides de 1 à 6 mm, avec un cratère central au sommet. Elles apparaissent sur le tronc, les aisselles, les membres et parfois sur le visage et les parties génitales. Très contagieuses, elles disséminent par autocontamination causée par le grattage. On les traite avec une curette ;
- les verrues séborrhéiques, qui devraient être appelées « kératoses séborrhéiques », sont des taches marron de squames grasses. Elles affectent essentiellement les personnes âgées et se décollent assez facilement. Elles ne sont pas d’origine virale. Le traitement classique est l’azote liquide à −196 °C. En cours de traitement, il ne faut pas s’exposer au Soleil. Des mutations d’un gène, FGFR3, qui code un récepteur aux facteurs de croissance, sont retrouvées dans 40 % de ces verrues.
Tabac
 Le tabac est un produit psychoactif manufacturé élaboré à partir de feuilles séchées de plantes de tabac commun (Nicotiana tabacum), une espèce originaire d’Amérique centrale appartenant au genre botanique Nicotiana (famille : Solanaceae).
Le tabac est un produit psychoactif manufacturé élaboré à partir de feuilles séchées de plantes de tabac commun (Nicotiana tabacum), une espèce originaire d’Amérique centrale appartenant au genre botanique Nicotiana (famille : Solanaceae).
Le tabac génère une forte dépendance et sa consommation est responsable de près de 6 millions de décès par an dans le monde dont 600 000 sont des non-fumeurs exposés à la fumée (tabagisme passif). De nombreuses maladies sont liées au tabagisme (maladies cardiovasculaires et cancers entre autres).
Production
Les Nicotiana sont des plantes néotropicales nitrophiles, originaires des régions chaudes et nécessitant un sol riche en humus. La température et la nature des sols jouent un rôle prépondérant sur les propriétés du tabac : la culture ne peut s’effectuer qu’entre des températures allant de 15 °C à 35 °C, 27 °C constituant un idéal pour l’épanouissement des plants.
On estime la surface cultivée mondiale à 5 millions d’hectares, essentiellement en Asie et en Amérique, bien que sa relative plasticité lui permette d’être cultivée entre le 60e degré de latitude nord et le 40e degré de latitude sud.
Le degré de maturation et la méthode de récolte des feuilles constituent des éléments essentiels et déterminants pour leur destination. Sous-maturées, les feuilles sont destinées aux capes pour cigares (l’enveloppe extérieure). La récolte en feuilles peut durer plus d’un mois, les feuilles étant récoltées une par une selon la maturation, tandis que la récolte par tige est beaucoup plus rapide car mécanisée, mais au détriment de la qualité. Il existe trois grandes variétés de tabac cultivé pour être fumé : le tabac de Virginie, le Burley (en) et le tabac oriental.
Composition
La composition du tabac est complexe (des études avancent un ordre de grandeur de 4 000 composés chimiques dont 40 reconnus carcinogènes), à cause de la complexité de la plante et à cause des nombreux traitements réalisés sur le tabac récolté pour en assurer la conservation, la couleur, le parfum, le goût, la plasticité, etc.
Dans la plante fraiche de Nicotiana tabacum, on trouve un mélange d’alcaloïdes composés de 93 % de (S)-nicotine, 3,9 % de (S)-anatabine, de 2,4 % de (S)-nornicotine, et de 0,5 % de (S)-anabasine. Lors de sa croissance, la plante absorbe plusieurs produits radioactifs, qu’on retrouvera dans la fumée, le filtre et moindrement le papier des cigarettes ou des bidies et dans les poumons, via l’inhalation de la fumée. Le polonium du tabac engendre le plus de radioactivité inhalée.
Les feuilles de tabac sont sensibles à certains polluants dont l’ozone troposphérique. Le stress oxydant peut en modifier la composition.
L’American Journal of Public Health (en) a montré, en septembre 2008, que les « majors » de l’industrie du tabac, Philip Morris (PM), RJ Reynolds, British American Tobacco, etc., ont volontairement caché au public, depuis les années 1960, la présence de polonium 210, une substance hautement cancérigène (et utilisée pour l’assassinat de l’espion Alexander Litvinenko) dans les cigarettes. Une des explications de cette présence de produits radioactifs dans le tabac est l’utilisation fréquente aux États-Unis d’engrais à base d’apatites, utilisés pour donner une saveur spécifique au tabac. Certaines variétés semblent absorber moins de radon et de polonium20 (sous réserve que cela ne soit pas dû à une moindre présence de ces produits dans leur environnement).
L’industrie tabatière ajoute en plus dans le tabac de cigarettes des additifs (arômes, sucres, humidifiants), notamment des composés d’ammoniac qui modifient le pH de la nicotine (plus alcalin), en facilitent l’absorption tout en renforçant la dépendance à celle-ci (ouverture plus importante des récepteurs à la dopamine).
Effets “ADDICTIFS”
La nicotine ne met que 7 secondes après chaque inhalation pour atteindre le cerveau, où elle provoque l’équivalent d’une mini-décharge d’adrénaline. Selon les individus, elle jouera le rôle d’accélérateur ou de frein :
- Pour les uns, elle stimule l’activité cérébrale, augmente la vigilance et les facultés de concentration intellectuelle. A chaque bouffée, elle provoque une accélération du pouls, une augmentation de la tension artérielle et du rythme cardiaque (de 8 à 10 pulsations par minute vingt-quatre heures sur vingt-quatre) ;
- Chez d’autres, au contraire, la nicotine a un effet tranquillisant et anxiolytique : elle contribue à inhiber les angoisses latentes en agissant comme un sédatif. La façon de fumer varie énormément d’un individu à l’autre. Car sans le savoir, le fumeur tire sur sa cigarette, son cigare ou sa pipe, pour obtenir le taux de nicotine que son organisme réclame. C’est le phénomène d’autotitration de la nicotine.
La nicotine est la principale substance responsable de la dépendance au tabac. Le phénomène d’accoutumance à la nicotine se produit dans le cerveau. Dès que la nicotine y arrive, elle stimule la libération de dopamine. Ce messager chimique joue un rôle clé dans la perception neurologique du plaisir. Il diminue l’anxiété, améliore l’humeur et la mémoire et réduit l’appétit.
Si l’on calcule que chaque cigarette permet environ 10 bouffées, une personne qui fume 30 cigarettes par jour envoie, quotidiennement, 300 appels de dopamine à son cerveau !
Des études suggèrent que le tabagisme diminue l’appétit, mais n’a pas conclu que les personnes en surpoids devraient fumer ou que leur santé amélioreraient par le tabagisme. Ceci est aussi une cause de coeur diseases.Smoking diminue également du poids en surexprimant le gène AZGP1 qui stimule la lipolyse.
Le plaisir neuronal, comme tous les plaisirs, n’a qu’un temps.
Chaque fois que la dopamine est relâchée, les récepteurs de dopamine sont mis en état d’alerte. Graduellement, leur sensibilité s’émousse et ils n’arrivent plus à se satisfaire du taux normal de dopamine : ils sont « en manque ». Le fumeur est tenté de fumer de plus en plus car une plus grande stimulation est nécessaire pour produire le même effet. La toxicomanie devient rapidement un problème chronique.
Toxicité
La consommation de tabac est responsable selon l’OMS de 6 millions de morts par an dans le monde, soit approximativement 10 % du total.
Le retentissement sur les organes vascularisés est évident. Un fumeur qui consomme un paquet de cigarettes par jour a une oxygénation équivalente à celle d’un non-fumeur à 2500 mètres d’altitude…
La consommation de tabac peut provoquer :
- des maladies cardiovasculaires : maladie coronarienne, accident vasculaire cérébral, anévrisme aortique, artériopathie oblitérante des membres inférieurs ;
- des cancers : cancer bronchique, cancer du larynx, cancer du pharynx, cancer de la bouche, cancer de la vessie, cancer de l’œsophage, cancer du rein, cancer du pancréas, cancer du col de l’utérus, cancer du sein ;
des maladies respiratoires broncho-pneumopathie chronique obstructive, aggravation de l’asthme, augmentation du risque de pneumonie, histiocytose X, syndrome d’apnée du sommeil ; - des maladies de la grossesse et de la petite enfance : placenta praevia, retard de croissance intra-utérin, mort subite du nourrisson, pathologies infectieuses bénignes ;
- des maladies digestives : œsophagite, reflux gastro-œsophagien, ulcère gastroduodénal, maladies du pancréas, aggravation d’une hépatite, aggravation de la maladie de Crohn ;
- des maladies variées : aggravation de la dégénérescence maculaire liée à l’âge, aggravation d’une kératite, aggravation de l’acné, retard de cicatrisation, pseudarthrose, agueusie, anosmie.
L’arrêt de la consommation de tabac permet de réduire les risques.
Mécanismes carcinogènes
La fumée contient plusieurs produits pyrolytiques cancérigènes qui se lient à l’ADN et provoquent des mutations génétiques. Les carcinogènes particulièrement puissants sont des hydrocarbures aromatiques polycycliques (HAP), qui sont toxiques jusqu’à mutagènes époxydes.
Il y a plus de 19 cancérigènes connus dans la fumée de cigarette.
Voici quelques-unes des substances cancérigènes les plus puissants :
- Les hydrocarbures aromatiques polycycliques (HAP) sont des composants de goudron produits par pyrolyse en couvant la matière organique et émis dans la fumée. Plusieurs de ces HAP sont déjà toxiques dans leur forme normale, cependant, beaucoup peuvent devenir encore plus toxiques pour le foie. En raison de la nature hydrophobe des HAP qu’ils ne se dissolvent pas dans l’eau et sont difficiles à expulser du corps. Afin de rendre les HAP plus solubles dans l’eau, le foie crée une enzyme appelée cytochrome P450 qui ajoute un atome d’oxygène supplémentaire à la HAP, le transformant en un époxyde mutagène, qui est plus soluble, mais aussi plus réactive. Le pouvoir cancérogène est radiomimétique, à savoir semblable à celui produit par les rayonnements ionisants nucléaires.
- Le premier HAP à être identifié comme cancérogène dans la fumée de tabac est le benzopyrène, qui a montré intoxiquer un époxyde qui se fixe de manière irréversible à l’ADN nucléaire d’une cellule, qui peut soit tuer la cellule ou causer une mutation génétique. Si la mutation inhibe la mort cellulaire programmée, la cellule peut survivre à devenir une cellule cancéreuse.
Les fabricants de tabac ont expérimenté avec la technologie de vaporisation pour permettre de consommer des cigarettes sans la formation de benzopyrènes cancérogènes. Bien que ces produits sont devenus de plus en plus populaires, ils représentent encore qu’une très petite fraction du marché, et aucune preuve concluante n’a été démontré pour prouver ou réfuter les allégations positives pour la santé positifs.
- Le premier HAP à être identifié comme cancérogène dans la fumée de tabac est le benzopyrène, qui a montré intoxiquer un époxyde qui se fixe de manière irréversible à l’ADN nucléaire d’une cellule, qui peut soit tuer la cellule ou causer une mutation génétique. Si la mutation inhibe la mort cellulaire programmée, la cellule peut survivre à devenir une cellule cancéreuse.
- L’acroléine, qui est abondant dans la fumée de tabac, se lie également de manière irréversible à l’ADN, cause des mutations et provoque donc aussi le cancer. Cependant, il n’a pas besoin d’activation pour devenir cancérigène. Il donne fumer une odeur âcre et un effet lacrymogène irritant et est un contributeur majeur à sa cancérogénicité. Comme métabolites des HAP, l’acroléine est également un agent alkylant électrophile et se lie à la base guanine de l’ADN, par une addition conjuguée, suivie d’une cyclisation dans un hémiaminal en permanence. Le produit d’addition acroléine-guanine induit des mutations d’ADN au cours de la reproduction, et donc provoque des cancers d’une manière similaire aux HAP. Cependant, l’acroléine est 1000 fois plus abondant que les HAP dans la fumée de cigarette et est en mesure de réagir comme il est, sans activation métabolique. Acroléine a été montré pour être un mutagène et cancérigène dans les cellules humaines. La cancérogénicité de l’acroléine a été difficile à étudier par l’expérimentation animale, car il a une telle toxicité qu’elle tend à tuer les animaux avant qu’ils ne développent un cancer.
Généralement, les composés capables de réagir par l’addition conjuguée comme agents électrophiles (ce qu’on appelle des accepteurs de Michael, après la réaction de Michael) sont toxiques et cancérigènes, car ils peuvent alcaliniser l’ADN en permanence, de manière similaire à du gaz moutarde ou de l’aflatoxine. L’acroléine est un seul d’entre eux présents dans la fumée de cigarette; par exemple, le crotonaldéhyde a été trouvée dans la fumée de cigarette. Michael accepteurs contribuent également à l’inflammation chronique présente dans la maladie du tabac. - Les nitrosamines sont un groupe de composés cancérigènes présents dans la fumée de cigarette, mais pas dans les feuilles de tabac non durcis. La formule des nitrosamines sur le tabac séché à l’air se produit pendant le processus de durcissement par une réaction chimique entre la nicotine et d’autres composés contenus dans la feuille non durcie et divers oxydes d’azote présents dans tous les gaz de combustion. Le passage à durcissement de feu indirect a été démontré pour réduire les niveaux de nitrosamines à moins de 0,1 partie par million.
La fumée secondaire du tabac, ou la fumée principale exhalée, est particulièrement néfaste. Parce que la fumée exhalée est à des températures plus basses que la fumée inhalée, les composés chimiques subissent des changements qui peuvent devenir plus dangereux. En outre, la fumée subit des changements à mesure qu’elle vieillit, ce qui provoque la transformation du composé NO vers le NO2 plus toxique. En outre, la volatilisation cause des particules de fumée de plus en plus petites, et donc plus facilement intégrées profondément dans les poumons d’une personne qui respire plus tard l’air.
Carcinogènes radioactifs
En plus de produits chimiques, des substances cancérogènes non radioactives, le tabac et la fumée de tabac contiennent de petites quantités de plomb-210 (210Pb) et le polonium-210 (210Po) qui sont tous deux des agents cancérigènes radioactifs. La présence de polonium-210 dans la fumée principale de cigarette a été mesurée expérimentalement à des niveaux de 0,0263 à 0,036 uCi (mBq 0.97-1.33), ce qui équivaut à environ 0,1 pCi par milligramme de fumée (4 MBq / mg ) ; ou environ 0,81 pCi de plomb-210 par gramme de fumée condensée sec (30 Bq / kg).
Les recherches menées par NCAR radiochimiste Ed Martell a suggéré que les composés radioactifs dans la fumée de cigarette sont déposés dans des «points chauds» où les tubes bronchiques se branchent, que le goudron de la fumée de cigarette est résistant à la dissolution dans le liquide pulmonaire et que les composés radioactifs mettent beaucoup de temps à devenir moins radioactifs avant d’être effacé par des processus naturels. A l’intérieur, ces composés radioactifs peuvent persister dans la fumée secondaire, et une plus grande exposition se produirait lorsque ces composés radioactifs sont inhalées pendant la respiration normale, qui est plus profonde et plus longue que lors de l’inhalation des cigarettes. Les dommages au tissu de protection épithélial en fumant augmente seulement la rétention prolongée des insolubles polonium-210 composés produits à partir de la combustion du tabac. Martell estime qu’une dose de rayonnement carcinogène de 80-100 rads est délivrée au tissu pulmonaire à la plupart des fumeurs qui meurent d’un cancer du poumon.
Fumer une moyenne de 1,5 paquets par jour donne une dose de rayonnement de 60-160 mSv /an, par rapport à vivre à proximité d’une centrale nucléaire (0,0001 mSv /an) ou le MSV 3.0 /dose moyenne annuelle pour les Américains. Certaines des apatites en Floride utilisées pour produire du phosphate pour les cultures de tabac U.S.A. contient l’uranium, le radium, le plomb 210 et le polonium-210 et le radon. La fumée radioactive du tabac fécondé cette façon est déposée dans les poumons et libère le rayonnement, même si un fumeur quitte l’habitude. La combinaison de goudron cancérigène et le rayonnement dans un organe sensible tel que les poumons augmente le risque de cancer.
En revanche, un examen de tabac cancérogènes de fumée publiés dans le Journal de l’Institut national du cancer 1999 stipule que «les niveaux de polonium-210 dans la fumée de tabac ne sont pas censés être assez grand pour avoir un impact significatif de cancer du poumon chez les fumeurs.» Dans 2011 Hecht a également déclaré que les «niveaux de 201Po dans la fumée de cigarette sont probablement trop faibles pour être impliqués dans l’induction du cancer du poumon …”
Nicotine
La nicotine, qui est contenue dans les cigarettes et autres produits du tabac fumés, est un stimulant et est l’un des principaux facteurs conduisant à continuer de fumer du tabac. La nicotine est une substance chimique psychoactive très addictif. Lorsque le tabac est fumé, la majeure partie de la nicotine est pyrolysé ; une dose suffisante pour provoquer la dépendance somatique légère et légère à forte dépendance reste psychologique.
La quantité de nicotine absorbée par le corps du tabac dépend de nombreux facteurs, y compris le type de tabac, que la fumée est inhalée, et si on utilise un filtre. Il y a aussi une formation d’harmane (un inhibiteur de la MAO, prescrite dans la dépression et la maladie de Parkinson) à partir de l’acétaldéhyde dans la fumée de cigarette, qui semble jouer un rôle important dans la dépendance à la nicotine probablement en facilitant la libération de dopamine dans le noyau accumbens, en réponse à des stimuli nicotine.
Selon des études réalisées par Henningfield et Benowitz, la nicotine est plus addictive que le cannabis, la caféine, l’éthanol, la cocaïne et l’héroïne lorsque l’on considère à la fois la dépendance somatique et psychologique. Toutefois, en raison des effets de sevrage plus forts de l’éthanol, de la cocaïne et de l’héroïne, la nicotine pourrait avoir un plus faible potentiel de dépendance somatique que ces substances. Environ la moitié des Canadiens qui fument actuellement ont essayé d’arrêter. La dépendance à la nicotine peut se produire dès cinq mois après le début du tabagisme.
L’ingestion d’un composé par le tabagisme est une des méthodes les plus rapides et efficaces de l’introduire dans le courant sanguin, en second après à l’injection, ce qui permet le retour d’information rapide permettant aux fumeurs d’adapter leur dosage. En moyenne, il faut environ dix secondes pour que la substance atteingne le cerveau. En raison de l’efficacité de ce système de distribution, de nombreux fumeurs se sentent dans l’incapacité de cesser de fumer.
Parmi ceux qui arrivent à cesser de fumer durant trois mois consécutifs sans succomber à la nicotine,
la plupart sont en mesure de rester sans fumée pour le reste de leur vie.
Bien que la nicotine joue un rôle dans les épisodes aigus de certaines maladies (y compris les accidents vasculaires cérébraux, l’impuissance et la maladie de coeur) par sa stimulation de la libération d’adrénaline, augmentant la pression artérielle, le rythme cardiaque, la respiration et les acides gras, le plus grave effet à long terme sont plus le résultat des produits du processus de combustion lente et continue. Cela conduit à l’élaboration de divers systèmes de délivrance de la nicotine, comme le timbre de nicotine ou de gomme à la nicotine, qui peuvent satisfaire le besoin addictif en livrant la nicotine sans la combustion sous-produits nocifs. Cela peut aider le fumeur fortement dépendant de quitter progressivement, tout en interrompant d’autres dommages à la santé.
Des données récentes ont montré que le tabagisme augmente la libération de dopamine dans le cerveau, en particulier dans la voie mésolimbique, le même circuit neuro-récompense activé par l’abus des drogues telles que l’héroïne et la cocaïne. Ceci suggère que l’utilisation de la nicotine a un effet agréable qui déclenche le renforcement positif. Une étude a révélé que les fumeurs présentent une meilleure réaction en temps et les performances de la mémoire par rapport aux non-fumeurs, ce qui correspond à une augmentation de l’activation des récepteurs de la dopamine. Neurologiquement, des études sur les rongeurs ont montré que l’auto-administration de nicotine abaissent les seuils de récompense. Cette augmentation de la sensibilité au circuit récompense persiste plusieurs mois après que l’auto-administration ait pris fin, ce qui suggère que la nicotine modifie la fonction de récompense du cerveau de manière longue ou permanente. En outre, il a été trouvé que la nicotine peut activer la potentialisation à long terme in vivo et in vitro. Ces études suggèrent que “la mémoire de trace” de la nicotine peut contribuer à des difficultés dans l’abstinence à la nicotine.
La cancérogénicité de la fumée de tabac n’est pas expliquée par la nicotine en soi, qui ne sont pas cancérigènes ou mutagènes, même si elle est un précurseur métabolique pour plusieurs composés qui le sont. En outre, le tabac inhibe l’apoptose, accélérant ainsi les cancers existants. Aussi, le NNK, un dérivé de la nicotine converti de la nicotine, peut être cancérigène.
Il est à noter que la nicotine, bien que fréquemment impliquée dans la production de la dépendance au tabac, n’est pas significativement addictive lorsqu’elle est administré seule. Le potentiel de dépendance se manifeste après la co-administration d’un inhibiteur de MAO(monoamine oxidase), ce qui provoque spécifiquement la sensibilisation de la réponse locomotrice chez le rat, une mesure du potentiel de dépendance.
Syndrome du sevrage tabagique
Irritabilité, anxiété, tristesse… les symptômes de manque peuvent être plus ou moins présents selon les individus. Mais il est prévisible d’en être victime durant les premières semaines suivant l’arrêt du tabac.
Pour une personne qui veut cesser de fumer, la perte de ces éléments véritablement positifs
du tabagisme (diminution de l’anxiété, amélioration de l’humeur et de la mémoire et réduction de l’appétit) est une étape cruciale à franchir.
D’autres facteurs émotifs et comportementaux accroissent la dépendance, comme le plaisir du geste et l’association avec des moments agréables (le premier café, le repas avec des amis, etc.).
Le sommeil, qui est souvent déjà de moins bonne qualité chez les fumeurs, est aussi fréquemment perturbé pendant quelques semaines. Les réveils sont plus courants durant la nuit. Il est habituel que les ex-fumeurs se lèvent une heure plus tôt le matin, durant la première semaine tout en ayant l’impression d’avoir mal dormi. Patience. Là aussi, tout reviendra peu à peu à la normale.
De nombreux cas de constipations, ballonnements, gastrites, ou crise de fringale… sont aussi à retenir et surtout à ne pas négliger !
Pour limiter l’apparition de tous ces phénomènes d’humeur, mieux vaut ne pas choisir le jour “J” dans une période d’intense activité professionnelle ou s’il y a des problèmes personnels ou une fragilité.
Les spécialistes du sevrage tabagique recherchent, notamment chez les gros fumeurs, la présence d’une anxiété ou de symptômes dépressifs. Ces derniers sont, en effet, deux fois plus répandus chez les fumeurs. Arrêter de fumer quand on présente une authentique dépression risquerait de la majorer et d’entraîner un déplacement vers d’autres formes de dépendance.
L’hygiène de vie joue un rôle essentiel pour lutter contre les manifestations désagréables du sevrage tabagique. Il est ainsi particulièrement recommandé de modérer sa consommation de café ou de thé, qui sont des excitants du système nerveux et accroissent l’anxiété. Attention aussi à l’alcool ou à la nourriture !
En revanche, la pratique d’une activité sportive aura l’avantage de calmer tout en
permettant de lutter contre la prise de poids favorisée par l’arrêt du tabac.
Fibromyalgie
L’étymologie du terme vient d’une part du latin fibra, « fibre », et d’autre part du grec ancien avec myos et algos, respectivement « muscle » et « douleur ». D’autres expressions peuvent désigner la même entité : syndrome polyalgique idiopathique diffus, fibromyosite, fibrosite, polyenthésopathie, fibromyalgie primitive.
La fibromyalgie, ou syndrome fibromyalgique, est une maladie associant des douleurs musculaires et articulaires diffuses, une fatigue, des troubles du sommeil, des troubles cognitifs mineurs et des troubles de l’humeur d’intensité variable et d’évolution chronique.
Cette maladie, fréquente, potentiellement invalidante, touche le plus souvent les femmes d’âge moyen. La cause est inconnue, et une anomalie de fonctionnement du système nerveux central est supposée. Il y aurait une sensibilisation excessive des récepteurs impliqués dans la perception de la douleur.
Les dernières découvertes scientifiques ont prouvé son aspect neurologique, lié à des déficiences en neurotransmetteurs comme la dopamine, la sérotonine et la noradrénaline. En 2006, des études démontrent par l’IRM fonctionnelle une activité anormale dans la partie du cerveau qui traite la douleur chez les fibromyalgiques, activité différente chez les personnes non atteintes.
Signes et symptômes
La fibromyalgie se présente sous forme d’un syndrome associant des douleurs diffuses, une fatigue, des troubles du sommeil, des troubles cognitifs mineurs et des troubles de l’humeur fluctuant avec le temps.
La douleur est habituellement le principal symptôme. Présente sur le long terme (au moins 3 mois) et de début insidieux, elle est ressentie au niveau des muscles et des articulations, et peut varier d’un jour à l’autre en termes de localisation et d’intensité. Elle peut être influencée par les conditions météorologiques et le stress. Le plus souvent, la douleur est provoquée à la pression.
D’autres douleurs peuvent être présentes, en rapport avec un syndrome de l’intestin irritable, une migraine, un syndrome prémenstruel chez la femme, un syndrome myofascial ou un syndrome algo-dysfonctionnel de l’appareil manducateur.
Diagnostic
Les diagnostics différentiels à évoquer sont d’autres causes de douleurs diffuses telles que des pathologies endocriniennes comme l’hypothyroïdie, des rhumatismes inflammatoires comme la polyarthrite rhumatoïde, des pathologies neurologiques comme la sclérose en plaques, des pathologies psychiatriques comme la dépression, ou encore des douleurs liées à la prise de certains médicaments comme les statines.
Les analyses biologiques simples pouvant être habituellement réalisées comportent un hémogramme, une mesure de la vitesse de sédimentation, un dosage de la protéine C réactive, de la créatine kinase et de la TSH afin d’éliminer si nécessaire certains diagnostics différentiels. La recherche d’anticorps antinucléaire, lorsqu’elle est faite, est parfois positive, sans porter à conséquence.
Liquide céphalo-rachidien
La découverte la plus systématiquement reproduite en laboratoire est une concentration haute, chez les sujets atteints, des niveaux en substance P, un neurotransmetteur lié à la perception de la douleur. La présence des métabolites servant à la formation des neurotransmetteurs monoamines, la sérotonine, la noradrénaline, et la dopamine — qui jouent tous un rôle dans l’analgésie naturelle du corps, a été prouvée comme étant anormalement basse, alors que la concentration des opiacés endogènes (comme l’endorphine et l’enképhaline) semble être plus haute que la normale. Une concentration élevée visible en facteur de croissance nerveuse (Nerve Growth Factor) a été prouvée. Cette substance est connue pour participer à la structuration et à la plasticité des interconnexions entre le cerveau et la moelle épinière. Il y a également des preuves d’une stimulation accrue des acides aminés au sein du liquide cérébro-spinal, avec une corrélation prouvée entre les niveaux des métabolites de glutamates et du monoxyde d’azote et la sensation de douleur.
Hyperactivité et hypoactivité
La preuve d’une réaction anormale du cerveau dans le cadre de la fibromyalgie a été prouvée par imagerie cérébrale fonctionnelle. Les premières découvertes font état d’une circulation sanguine diminuée dans le thalamus, des ganglions de la base et de certaines zones médianes du cerveau. Comparativement à des personnes saines, ces zones sont moins actives (hypoactivité) à douleur égale, et ont une activation différée, dans la réaction à la douleur. Certaines zones du cerveau montrent en revanche une hyperactivité des patients à la stimulation douloureuse, en particulier les zones liées à la douleur comme le cortex somatosensoriel primaire et secondaire, le cortex insulaire et le cortex cingulaire avant. Les patients démontrent également une activité neuronale anormale dans les zones du cerveau associées à la perception de la douleur associée à des stimulus non douloureux (douleur psychique par exemple), comme dans le cortex préfrontal, le cortex prémoteur, le cortex insulaire, les cortex cingulaires.
Des preuves d’une mal-fonction de l’hippocampe, indiquant la présence réduite en métabolites ont aussi été trouvées par des études utilisant l’imagerie par résonance magnétique. Une corrélation significative a été démontrée entre la densité de ces métabolites et un index de sévérité de la douleur clinique couramment utilisé.
Concentrations en neurotransmetteurs
La corrélation entre la gravité de la douleur clinique ressentie et la concentration d’un acide aminé neurotransmetteur stimulant, le glutamate, a également été démontrée par IRM. Une accélération de l’atrophie habituellement liée à l’âge a été démontrée en utilisant une morphométrie basée sur des voxels (voxel-based morphometry, VBM) avec des zones de matière grise plus réduites que la normale dans le cortex cingulaire, le cortex insulaire et le gyrus parahippocampal.
Des études utilisant la tomographie par émission de positons ont démontré une synthèse réduite de la dopamine dans le tronc cérébral et le centre du système limbique50. Une corrélation entre la gravité de la douleur et le manque de dopamine synthétisée a également été démontrée dans le cortex insulaire. Une étude démontra par la suite, qu’après un stimulus douloureux, la synthèse réactive en dopamine était déréglée et retardée de façon flagrante, dans les ganglions de la base. Cette étude est confirmée par un lien entre les “18 points douloureux” reconnus par l’ARC et la dopamine D2 moins disponible, spécifiquement dans le putamen droit. Enfin, une disponibilité moins grande des récepteurs opioïdes dans le Striatum, le prosencéphale et le cortex cingulaire a été démontrée, avec un lien entre la sensation de douleur, et l’absence de récepteurs disponibles dans le nucleus accumbens.
Des études génétiques récentes tentent à confirmer le lien entre les gènes de synthèse de certains neurotransmetteurs et la fibromyalgie.
Troubles du sommeil
Les premières découvertes objectives associées à la maladie ont été rapportées en 1975 où a été démontrée la présence d’ondes alpha (associées usuellement à des phases de sommeil léger) anormales en phase 4 (sommeil profond) durant l’Électro-encéphalogramme de patients fibromyalgiques. En fait, en interrompant le sommeil de phase 4 constamment sur des sujets jeunes et en bonne santé, Moldofsky et son équipe ont été capables de reproduire une tension musculaire supposée comparable à celle des patients fibromyalgiques. Cependant ces sensations ont disparu lorsque les sujets ont pu retrouver un sommeil normal.
Depuis cette étude, de nombreuses études confirment des anomalies du sommeil variées dans des sous-groupes de patients fibromyalgiques.
Sensibilité polymodale
Plusieurs études résultant de stimulation expérimentale ont démontré que les patients fibromyalgiques démontrent une sensibilité accrue à la pression, aux sensations de chaleur et de froid, à des stimulations électriques et chimiques. Des expérimentations sur les systèmes régulateurs de la douleur ont montré que les patients atteints de fibromyalgie montrent aussi une dérégulation de différents mécanismes inhibiteurs de la douleur. Elles démontrent également une réaction exagérée à un stimuli répété et la diminution ou l’absence de la réaction analgésique induite par l’effort physique. Ensemble, ces résultats pointent vers un dérèglement du système nerveux central.
Perturbation neuroendocrinienne
Les études de patients atteints de fibromyalgie ont démontré des anomalies dans les fonctions neuroendocriniennes usuelles comme une hypocortisolémie, une sécrétion excessive de l’hormone corticotrope en réponse à une stimulation, et une résistance au feedback glucocorticoïde. Une réduction progressive de la présence d’hormone de croissance humaine a aussi été démontrée sur certains groupes de patients, alors que la plupart démontrent des sécrétions hormonales diminuées face à des efforts physiques intenses ou à des stimulations pharmaceutiques. D’autres anomalies incluent un temps de réponse réduit de la thyréostimuline et des hormones thyroïdiennes lors de stimulations hormonales. Une hausse relativement élevée des niveaux de prolactine, avec une désinhibition de la sécrétion de prolactine lors de stimulations hormonales et une sécrétion insuffisante des hormones produites par les glandes surrénales, a également été constatée.
Ces changements pourraient être attribués aux effets du stress chronique que cause la maladie qui, après avoir été reçu et traité par le système nerveux central, activent la sécrétion d’hormones neuronales corticotrophines hypotalamiques. Cela résulterait en une perturbation de la communication Hypophyse-Glande Surrénale et en un excès en somatostatine hypothalamique qui en retour inhibent la sécrétion d’un certain nombre d’autres hormones.
Hyperactivité du système nerveux sympathique
Une analyse a démontré une activité perturbée et excessive du système nerveux sympathique avec une réactivité des glandes sympathiques réduite à différents facteurs de stress, qu’ils soient physiques ou mentaux. Les patients atteints de fibromyalgie ont une variabilité de leur rythme cardiaque bas, cet index de l’équilibre sympathique/parasympathique indiquant une hyperactivité sympathique soutenue, en particulier de nuit. De plus, les niveaux en neuropeptide Y (NPY) dans le plasma sanguin sont bas chez les malades, ce neuropeptide étant localisé avec la noradrénaline dans le système nerveux sympathique. À l’inverse les niveaux circulatoires d’adrénaline et de noradrénaline ont été parfois décrits comme hauts, bas et normaux.
L’injection d’interleukine 6 (une cytokine capable de stimuler la production d’hormone de sécrétion de corticotropine hypotalamique qui, à son tour, stimule l’activité du système nerveux sympathique) provoque une hausse forte des niveaux circulatoires de noradrénaline et une hausse du rythme cardiaque. Ces hausses sont plus fortes chez les patients fybromyalgiques que chez les personnes saines.
Facteurs aggravants
Les symptômes de la fibromyalgie seraient notoirement dans les conditions suivantes, liés au stress, et peuvent déclencher des réactions au niveau des neurotransmetteurs ou des hormones :
- traumatisme, stress et choc émotionnel ;
- autre maladie ;
- bruit ;
- entourage de personnes ;
- manque de protéines dans l’alimentation ;
- quantité de nourriture insuffisante ;
- mauvaise gestion du sommeil (quantité insuffisante ou excessive) ;
- fatigue ou effort physique trop important ;
- chaleur et canicule ;
- froid ;
- utilisation de produits influant sur les neurotransmetteurs.
Pour certains patients les cycles correspondent à :
- une barosensibilité – réaction aux changements de la pression atmosphérique ;
- une hygrosensibilité – réaction au taux d’humidité ;
- une thermosensibilité – réaction à la température.
On parle globalement d’hypersensibilité.
Fatigue chronique
Aux symptômes courants s’associe souvent une fatigue dite « chronique » réactionnelle (à ne pas confondre avec le syndrome de fatigue chronique, que peuvent avoir en plus certains fibromyalgiques). Cette fatigue est décrite comme réactionnelle car fluctuante selon l’environnement et les circonstances, pouvant disparaître totalement puis réapparaître. Le syndrome de fatigue chronique n’est pas lié à un excès de substance P. Les mécanismes responsables de la douleur sont donc probablement différents pour ces deux conditions.
Causes supposées

À partir de 2000-2004, les scientifiques se penchent de plus en plus vers des désordres de nature neuronaux, immuno-chimiques ou environnementaux, compte tenu de la résurgence surprenante de cas. Une atteinte du système nerveux central et un dérèglement neuronal ont été largement constatés chez les fibromyalgiques. Il semble exister une perception différente de la douleur chez le fibromyalgique, avec en particulier, un seuil de perception plus bas. Le mécanisme de ce fait est toujours débattu, mais lourdement supposé lié aux neurotransmetteurs responsables du traitement de la douleur.
Il est possible que les différentes variantes de fibromyalgie soient liées à une combinaison d’une ou plusieurs de ces causes supposées.
Prédisposition génétique
Outre le fait que cette maladie touche beaucoup plus de femmes que d’hommes, il existe de nombreuses preuves qu’un facteur génétique puisse jouer un rôle important dans le développement de la fibromyalgie. Par exemple, il existe beaucoup de familles présentant plusieurs personnes atteintes. Le mode de transmission est encore inconnu mais est probablement génétique. Les recherches ont démontré que la fibromyalgie est associée à des variations (ou polymorphisme) sur les gènes de production de la sérotonine, dopamine et catécholamine. Cependant ces polymorphismes ne sont pas spécifiques à la fibromyalgie, et sont associés à une variété d’autres maladies (comme le syndrome de fatigue chronique, syndrome du côlon irritable) et certaines formes de dépression.
Enfin nombre d’équipes sont sur la piste des gènes éventuellement déficients :
- une étude turque a démontré un lien entre des polymorphismes génétiques liés à la synthèse de la catéchol-O-méthyltranférase (COMT), et une prédisposition à la fibromyalgie ;
- une étude de l’équipe du professeur Vargas-Alarcón (sur des femmes saines et atteintes de fibromyalgie espagnoles et mexicaines) tend à prouver des liens entre la fibromyalgie et un polymorphisme des gènes codant pour les deux récepteurs adrénergiques alpha-AR et beta-AR. L’étude portant sur trop peu de cas, et des populations pas assez variées, doit être confirmée. De plus ces polymorphismes ne se retrouvent pas à 100 % dans les populations concernées. Toutes ces études confortent par contre le lien avec la synthèse déficiente de certains neurotransmetteurs.
On s’oriente donc vers la possibilité qu’un groupe de gènes déficients perturbent la synthèse des neurotransmetteurs liés à la douleur, prédisposant ainsi à la fibromyalgie. Le nombre et l’importance des gènes atteints détermineraient ainsi la sévérité de la maladie.
Dérèglement des neurotransmetteurs
Une déficience dans certains neurotransmetteurs (excès de substance P, manque de sérotonine et de noradrénaline) a été identifiée. L’excès de substance P est reconnu pour provoquer une hyperalgésie une réduction de la sérotonine ou de la noradrénaline produit également une hyperalgésie par la réduction des systèmes inhibiteurs de la douleur.
Les taux plus élevés d’anticorps anti-sérotonine dans le sang, de facteurs de croissance dans le liquide céphalo-rachidien et des variations du système de réponse inflammatoire viennent corroborer cette hypothèse. Certains docteurs posent désormais clairement l’existence d’une composante auto-immune de la fibromyalgie.
Un lien a également été prouvé entre fabrication des monoamines et fibromyalgie. Des gènes, responsables de la fabrication des monoamines, ont été identifiés comme déficients. Ces monoamines comprennent la sérotonine et les catécholamines, qui servent à fabrication de la dopamine, de l’adrénaline et de la noradrénaline. Ces neuromédiateurs, substances ayant un rôle pour transmettre l’influx nerveux et qui influent sur l’anxiété, le stress et le moral, seraient en nombre insuffisant chez les fibromyalgiques.
Dérèglement immunologique
D’autres études tentent à démontrer que les cytokines, impliquées dans le système immunitaire auraient une action perturbée chez les personnes atteintes de fibromyalgie. Il existerait donc une cause de survenue de la fibromyalgie mettant en cause un phénomène immunologique en relation étroite avec un phénomène neurologique. Ces études, restant à être confirmées, car portant sur un nombre réduit de patients, prouvent que ces personnes atteintes de fibromyalgie ont un excès en cytokine, qui peut provoquer un excès en substance P. Le niveau de cytokine observé augmenterait avec la durée de la maladie.
On remarque également des niveaux de cytokine élevés chez les personnes manquant de sommeil. Il est donc actuellement impossible de déterminer si le manque de sommeil des fibromyalgiques est à l’origine de ce niveau de cytokine, ou si le taux de cytokine est à même de provoquer les maux, et donc l’absence de sommeil.
Irrigation du cerveau
Fin 2008, une équipe de chercheurs du Centre hospitalo-universitaire de la Timone à Marseille, dirigée par le professeur Eric Guedj, a identifié une anomalie au niveau de la circulation sanguine dans le cerveau de patients atteints de fibromyalgie, grâce à une tomographie à émission de photons (SPECT). L’étude a permis de découvrir que chez les patients atteints de fibromyalgie, certaines régions du cerveau sont trop irriguées, alors que d’autres le sont insuffisamment. Cette irrégularité modifie la manière dont le patient ressent et traite la douleur. Les chercheurs ont en outre identifié des liens entre le flux sanguin de certaines zones du cerveau et l’anxiété, les douleurs intempestives, le handicap et la dépression nerveuse. Les chercheurs ont identifié une augmentation de la circulation du sang dans certaines zones du cerveau qui servent à ressentir la douleur, alors qu’une diminution du flux sanguin a été identifié dans une autre zone chargée de la réponse émotionnelle à la douleur.
Troubles du sommeil
Des études d’électro-encéphalographie du sommeil ont prouvé que les personnes atteintes de fibromyalgie manquent de la phase de sommeil profond, et que les circonstances influant le sommeil de phase 4 (douleur, dépression, manque de sérotonine, certains médicaments, anxiété…) peuvent causer ou aggraver la maladie110. Selon cette hypothèse d’une perturbation du sommeil, un évènement, tel un traumatisme, peut causer une perturbation du sommeil, causant la douleur initiale du processus.
Cette hypothèse repose sur l’hypothèse que le sommeil de stage 4 est critique pour le fonctionnement du système nerveux, sachant que certains processus neurochimiques redémarrent durant cette phase. En particulier, la douleur cause la sécrétion d’une neuropeptide, la substance P dans la moelle épinière qui a pour effet d’amplifier la douleur et rend les nerfs plus sensibles à la douleur. Dans des circonstances normales, les zones autour d’une blessure deviennent plus sensibles à la douleur, mais si la douleur devient chronique, ce processus peut dérailler et s’étendre.
Cette hypothèse repose sur l’hypothèse que le sommeil profond permettrait de réinitialiser le mécanisme de la substance P, et qu’un manque de sommeil pourrait alors devenir une cause de la maladie.
Hormone de croissance humaine
Une hypothèse alternative suggère que des problèmes induits par le stress, dans l’hypothalamus, peuvent conduire à un sommeil réduit et réduit la production d’hormone de croissance humaine durant le sommeil profond. Les gens atteints de fibromalgies tendent à produire des niveaux inadéquats de cette hormone. Cette théorie est supportée par le fait que plusieurs substances, qui sont produites sous le contrôle direct ou indirect de cette hormone (comme IGF-1, cortisol, leptine et le neuropeptide Y) atteignent des niveaux anormaux avec les personnes atteintes de fibromyalgie111. De plus, des traitements avec injection d’hormone de croissance réduisent la douleur induite par la maladie, et permettraient l’obtention de sommeil profond ; l’influence de l’hormone de croissance fait encore débat, d’autres études ne faisant pas cas d’un manque de cette hormone chez d’autres patients.
Dérèglement hormonal lié au stress
Des études montrent que le stress est un facteur aggravant significatif dans le développement de la fibromyalgie.
En conséquence il a été avancé que la fibromyalgie puisse résulter d’un dysfonctionnement induit par le stress, notamment dans la fonction et l’intégrité de l’hippocampe. Cettre proposition est basée sur des études pré-cliniques sur des singes, qui ont montré que l’exposition à un stress psychosocial peut avoir des conséquences physiques sur les tissus du cerveau, incluant de l’atrophie et des changements métaboliques de l’hippocampe.
Cette hypothèse est soutenue par deux études qui ont utilisé l’imagerie par résonance magnétique pour trouver des anomalies métaboliques dans l’hippocampe de patients atteints de fibromyalgie, avec une corrélation significative entre anomalies et sévérité des symptômes cliniques. Il est actuellement impossible de déduire si le stress a provoqué la malformation de l’hippocampe, ou si la maladie est la cause de la malformation.
Un autre mécanisme reconnu est le dérèglement de l’axe hypothalamus-hypophyse-glande surrénale qui influe sur le stress, et peut provoquer une variation cyclique des symptômes.
Neurotransmetteurs d’origine dentaire
Tandis que les mâchoires semblent rétrécir, la taille semble s’allonger. Les dents ont donc moins de place et la dysharmonie dento-maxillaire devient très fréquente. L’éruption dentaire, qui est un mécanisme physiologique, nécessite à présent l’aide orthodontique car elle ne peut plus se réaliser spontanément. Les habitants des pays dits civilisés semblent avoir perdu cette capacité, alors que l’alignement se faisait encore spontanément dans la génération précédente. Les neuro médiateurs dont le chef de file est la substance P pourraient exprimer dans l’ensemble du corps la souffrance de la dysharmonie dento-maxillaire.
Autres hypothèses
D’autres hypothèses ont été avancées, comme :
- certaines toxines dans l’environnement du patient ;
- une cause virale comme le virus d’Epstein-Barr ;
- une réaction immunitaire anormale à une bactérie intestinale ;
- une érosion de la gaine chimique autour des nerfs sensoriels ;
- une dérégulation de la vasomotricité résultant en une ischémie des muscles ou une circulation sanguine anormale ;
- une dégradation de la posture causée par la dysfonction de l’articulation temporo-mandibulaire, elle-même due à une occlusion dentaire défectueuse. L’épuisement généré par les contractures musculaires résultant d’une posture vrillée contribuerait au syndrome de fatigue chronique rendant tout effort musculaire pénible, voire impossible.
- le syndrome ASIA y fait référence. Ces maladies ont toutes un vecteur commun la présence d’un corps étranger ou un adjuvant vaccinal en contact dans les tissus sur une période prolongée.
TRAITEMENTS ALLOPATHIQUES
Analgésiques et antidépresseurs : antidouleurs ou des antidépresseurs (classe des tricycliques) ou des antiépileptiques (antalgiques sur le système nerveux central)
Vu qu’il s’agit d’une maladie touchant une population étendue (2 à 5 % de la population mondiale) et très probablement dépendante à vie du médicament, des sommes d’argent colossales sont en jeu.
Les médicaments présentés ci-après ont des effets secondaires lourds :
Lyrica : antiépileptique constitué d’une molécule portant le nom de prégabaline
Neurontin : antiépileptique constitué d’une molécule portant le nom de Gabapentine
Duloxétine (Cymbalta/Xeristar)
Milnacipran : traitement de la dépression sous le nom commercial Ixel
Naltrexone
Jambes lourdes
Chevilles gonflées, jambes pesantes, picotements, sensation de chaleur, marbrures, varices… La mauvaise circulation est banale et fréquente, mais elle fait souffrir et peut s’aggraver.
L’insuffisance veineuse
En France, selon les statistiques Insee, 18 millions d’adultes se plaignent de lourdeurs et de douleurs dans les jambes, signes évocateurs d’insuffisance veineuse superficielle. Soit une femme sur deux et un homme sur quatre. C’est donc une pathologie fréquente et plus encore passé l’âge de 60 ans.
Pourtant, six Français sur dix à risque, de par leur hérédité ou leur métier par exemple, ignorent qu’ils sont concernés et ne prennent donc pas les mesures qui s’imposent pour éviter d’avoir des troubles veineux ou ralentir leur évolution. En fait, tant qu’on n’a pas de varices, on a tendance à négliger ses jambes.
Or, contrairement à une idée répandue, la maladie veineuse ne se signale pas systématiquement par leur présence. On peut souffrir d’insuffisance veineuse, jambes lourdes et enflées, fourmillements, rougeurs, sans avoir de varices.
L’insuffisance veineuse est l’incapacité des veines à faire remonter convenablement le sang des pieds vers le cœur. Contrairement aux artères, constituées de fibres élastiques, les parois des veines sont peu extensibles, beaucoup plus minces et contiennent moins de tissus musculaires. Pour assurer le retour veineux, les veines disposent de valvules antireflux, sortes de petits clapets disposés le long des parois, qui empêchent le sang de redescendre. Mais ils peuvent se détériorer…
La pression plantaire au cours de la marche pousse aussi le sang veineux, c’est la chasse plantaire, relayée par la contraction des mollets. Encore faut-il marcher…
A savoir : les hommes consultent moins et plus tard que les femmes parce que les varices sont invisibles sous les pantalons et qu’ils sont moins concernés par des préoccupations esthétiques. Ils consultent quand ils ont vraiment mal ou qu’ils ont déjà des complications.
Identifier les causes et les risques d’insuffisance veineuse
Quand les parois veineuses manquent de tonus et que les valvules fonctionnent mal, le sang ne remonte pas correctement et stagne de plus en plus, les veines se dilatent peu à peu et les tissus qui les entourent gonflent.
De l’œdème à la varice
Au début, les symptômes, jambes lourdes et enflées, picotements, crampes sont supportables et se manifestent par temps chaud ou après une journée passée debout. Mais avec les années, ils deviennent plus douloureux et plus fréquents. Des varicosités, petites lignes rouges et violettes sous la peau, apparaissent ou, plus inesthétiques encore, des varices. C’est trop souvent à ce stade ou pire, à celui des complications, que l’on s’inquiète.
Les grandes causes de l’insuffisance veineuse
Impossible malheureusement d’agir sur ces trois grands facteurs d’insuffisance veineuse.
- L’âge : Les veines vieillissent aussi et le risque d’avoir des varices augmente.
À 35 ans, 15 % de la population ont des varices, pour 65 % à 75 ans. - Le sexe féminin : Les veines des femmes ont sur leurs parois des récepteurs hormonaux qui les rendent sensibles aux modifications hormonales, puberté, pilule, grossesse, ménopause. Pendant la grossesse, s’ajoutent la compression des veines abdominales et pelviennes par l’utérus et une augmentation du volume sanguin.
- L’hérédité : Quand les deux parents ont des varices, les enfants en souffrent à leur tour dans 90 % des cas ; avec un seul parent, le risque est de 25 % pour les garçons et de 62 % pour les filles.
Le mode de vie, facteur d’insuffisance veineuse
D’autres facteurs, qui tiennent au mode de vie, favorisent ou aggravent l’insuffisance veineuse.
- Professions à risque : Ce sont celles qui obligent à piétiner, à rester longtemps debout ou assis(e), dans une atmosphère chaude et humide, ou à porter des charges lourdes : coiffeur(se), infirmier(e), hôtesse de l’air ou steward, serveur(se), vendeur(se), mais aussi cuisinier(e), boulanger(e)…
- Voyages de longue durée : Surtout ceux en avion. Rester assis(e) plus de 3 ou 4 heures sur un siège étroit et les jambes sous le menton gêne le retour veineux. De plus, la déshydratation due à la dépressurisation et la sécheresse de l’air influent sur la concentration du sang.
- Certains sports : Tous ceux qui entraînent des à-coups violents et nécessitent une contraction des muscles en respiration bloquée ou en apnée : tennis, squash, escrime, trampoline, haltérophilie, basket-ball, judo…
- Sédentarité : Ne pas bouger ou marcher assez compromet la chasse plantaire.
- Chaleur et soleil : La chaleur provoque une dilatation des veines qui empêche les valvules de remplir leur rôle, ainsi que l’exposition prolongée au soleil et les bains chauds.
- Surpoids et obésité : Les kilos en trop pèsent sur le réseau veineux.
- Tabagisme : Le tabac affaiblit la tonicité des veines.
Les complications en cas d’insuffisance veineuse
- Varices : Elles s’aggravent, différemment selon les personnes, en l’absence de traitements adaptés.
- Dermite ocre : La peau mal oxygénée s’asphyxie peu à peu et devient brunâtre.
- Hypodermite scléreuse : Les plaques évoluent vers une inflammation des tissus sous-cutanés et prennent un aspect cartonné. La peau est si fine qu’au moindre choc, l’ulcère peut survenir.
- Eczéma variqueux : Il provoque démangeaisons, desquamation et suintement qui peuvent, sans traitement (crème corticoïde), donner un ulcère.
- Ulcère variqueux : Il faut réagir vite pour éviter qu’il ne se creuse.
Le traitement cicatrisant est long (pansements hydrocolloïdes). Quand la plaie fait mal, car infectée, antibiotiques et corticoïdes sont indispensables. - Thrombose veineuse, ou phlébite : Autre conséquence grave du ralentissement du flux veineux. Toutes les varices ne provoquent pas de phlébite, mais elles la favorisent.
- Phlébite : Le sang coagule, bouche la veine et forme un caillot. La veine est dure, rouge, chaude et la jambe douloureuse. Consulter rapidement pour mettre en route un traitement et éviter que le caillot migre, remonte vers le cœur et bouche une artère pulmonaire.
- Embolie pulmonaire : C’est une complication gravissime. Au moindre doute, allez à l’hôpital.
Insuffisance veineuse : soulager et éviter les complications
Même si vous n’avez pas encore de signes visibles sur les jambes, inutile de souffrir et de risquer une aggravation. Prenez-les en mains.
Les vertus des plantes : Petit houx, marronnier d’Inde, fragon, hamamélis, vigne rouge, cassis, ginkgo biloba, myrtille…
Ces plantes sont reconnues de longue date pour leurs effets bénéfiques sur la circulation sanguine.
- Plantes veinotoniques en tisanes, gélules, comprimés, ampoules, solutions buvables. Appelés aussi phlébotoniques, ils sont utiles l’été en cures de 2 à 3 mois voire plus longtemps. Ils soulagent en stimulant le tonus veineux et peuvent aussi avoir une action locale sur l’inflammation, responsable de douleur et d’œdème.
Ils associent le plus souvent plusieurs plantes, aux actions complémentaires. - Gels et crèmes : Ils contiennent les mêmes composants issus de plantes et en plus, menthol, menthe poivrée ou camphre. A appliquer 2 ou 3 fois par jour en massages circulaires, en remontant du bas vers le haut de la jambe. Ils apportent un soulagement et une sensation de fraîcheur, appréciée l’été. Les conserver au réfrigérateur renforce l’effet froid.
- Indispensable compression : Elle consiste à appliquer sur les jambes ou segments de jambe, chaussettes, bas jarret ou autofixants, collants, aujourd’hui esthétiques, voire bandes, constitués d’un tissu ou d’un tricot élastique.
Contrairement aux veinotoniques, la compression, dégressive de la cheville vers la cuisse, ne soulage pas seulement les symptômes, mais prévient aussi les complications ou les traite. À ce titre, elle est prise en charge par l’Assurance maladie sur prescription. À chaque stade de la maladie correspond une classe, de la classe 1 à la classe 4, compression extra-forte.
Certaines gammes sont plus perfectionnées et plus élégantes (coloris, matière, motif).
Le thermalisme :
Les eaux thermales ont des effets bénéfiques à tous les stades de la maladie veineuse, au stade prévariqueux, dans les complications cutanées, hypodermite, ulcère, séquelles d’ulcère, et les séquelles de phlébite. Elles améliorent le retour veineux, réduisent œdèmes et douleurs, favorisent la cicatrisation. Les soins sont répartis en cure d’hydrothérapie interne, cures de boissons à base d’eau thermale, et externe, bains, jets hydromassants en immersion, couloirs de marche, massages sous affusion…
Principales stations spécialisées en phlébologie : Rochefort-sur-Mer et Jonzac (Charente-Maritime), Argelès-Gazost (Hautes-Pyrénées), La Léchère-les-Bains (Savoie), Bagnoles-de-l’Orne (Orne), Dax (Landes).
Jambes lourdes : les bons gestes
- Surélevez vos pieds en fin de journée : Idéalement, placez-les contre un mur à 90° pendant un quart d’heure. Vous inversez ainsi les effets de la pesanteur.
- Placez des cales de 5 à 10 cm sous le lit, côté pieds. Vous pouvez aussi investir dans un lit de relaxation qui permet de les soulever.
- Terminez la douche par un jet d’eau fraîche sur les jambes. Remontez des pieds jusqu’aux mollets ou trempez vos pieds jusqu’en haut des chevilles dans une bassine d’eau froide.
- Pratiquez une activité physique régulière qui favorise le retour veineux, marche, vélo. Pensez aussi à la natation, car l’eau exerce un massage qui allège le bas du corps et améliore la circulation sanguine.
- À la mer, marchez dans l’eau jusqu’aux genoux. Vous profitez de la fraîcheur de l’eau et de ses oligoéléments, et ce massage active le retour veineux.